سیستم های انرژی در ورزش: ۲-گلیکولیز بی هوازی و هوازی
نویسنده: علیرضا نیک نام (متخصص فیزیولوژی ورزشی)
آدرس صفحه اینستاگرام: Sportphysiologist@ آدرس ایمیل: Alireza73.Niknam@gmail.com
گلیکولیز بی هوازی
گلیکولیز یا مسیر امبدن – میرهوف (Embden–Meyerhof–Parnas) مجموعهای از واکنشهای درون سلولی است که توسط آن یک قند شش کربنه (معمولاً گلوکز-۶-فسفات) به ترکیبات کربندار کوچکتری (دو مولکول سه کربنه پیروات) شکسته میشود و بخشی از انرژی آزاد قند را تولید می کند. در فعالیت های ورزشی که با حداکثر تلاش بین ۳۰ ثانیه تا ۳ دقیقه به طول می انجامند سیستم گلیکولیز بی هوازی بیشترین نقش را در تامین انرژی مورد نیاز ورزشکار دارد. مانند دو ۴۰۰ و ۸۰۰ متر سرعت.
گلیکولیز یک واژه مرکب یونانی است که از دو بخش glykys به معنای شیرین و lysis به معنای شکستن (گلیکولیز: شکستن قند یا همان قندکافت) تشکیل شده است. نام امبدن –میرهوف از نام دو زیستشیمیدان آلمانی کاشف آن، یعنی گوستاو گورگ امبدن و اتو فریتز میرهوف گرفته شدهاست. در این واکنشها گلوکز ابتدا در گروه هیدروکسیل کربن شماره شش، فسفردار شده و گلوکز ۶-فسفات تشکیل می شود. آنزیم کلیدی که این واکنش را کاتالیز می کند هگزو کیناز نام دارد.
گلوکز ۶ فسفات در مرحله بعدی به فروکتوز ۶-فسفات تبدیل میگردد. سپس این ترکیب در کربن شماره یک نیز فسفرگیری کرده و فروکتوز ۶،۱- بیسفسفات را تولید میکند. در هر دو واکنش فسفرگیری، ATP دهنده گروه فسفاتی است. بنابراین اگر مبدا گلیکولیز از گلوکز باشد، برای اینکه فرایند گلوکولیز پیش برودنیازمند مصرف ۲ مول ATP یا انرژی است. با این حال سلول های عضلانی می توانند از قند ذخیره خود یعنی گلیکوژن نیز استفاده کنند. در هنگام فعالیت های ورزشی شدید، تارهای عضلانی گلیکوژن را به واحد های گلوکز ۱ فسفات تجزیه می کنند و سپس گلوکز ۱ فسفات به فروکتور ۶ فسفات تبدیل می شود.
این فرایند گلیکوژنولیز نام دارد. ارزش آن این است که در گلیکوژنولیز برای تشکیل فروکتوز ۶ فسفات نیازی به مصرف ATP نیست. بنابراین اگر مبدا گلیکولیز بی هوازی از گلیکوژن باشد یک ATP کمتر هزینه می شود. آنزیمی که گلیکوژن را به گلوکز ۱ فسفات تبدیل می کند، گلیکوژن فسفوریلاز نام دارد.
کلمات کلیدی: گلیکولیز، گلیکولیز بی هوازی، اسید لاکتیک، سیستم های انرژی در بدن
در ادامه فروکتوز ۶،۱-بیسفسفات به مولکولهای دیهیدروکسی استون فسفات و گلیسرآلدهید ۳-فسفات میشکند که دیهیدروکسی استون فسفات نیز طی یک واکنش تعادلی آنزیمی به گلیسرآلدهید ۳-فسفات تبدیل میشود. از ابتدای گلیکولیز تا تکشیل گلیسروآلدئید ۳ فسفات را بخش اول گلیکولیز (هزینه ATP) می نامند و بعد از آن را بخش دوم گلیکولیز و مراحل تشکیل ATP (بازپرداخت بدهی) می نامند.
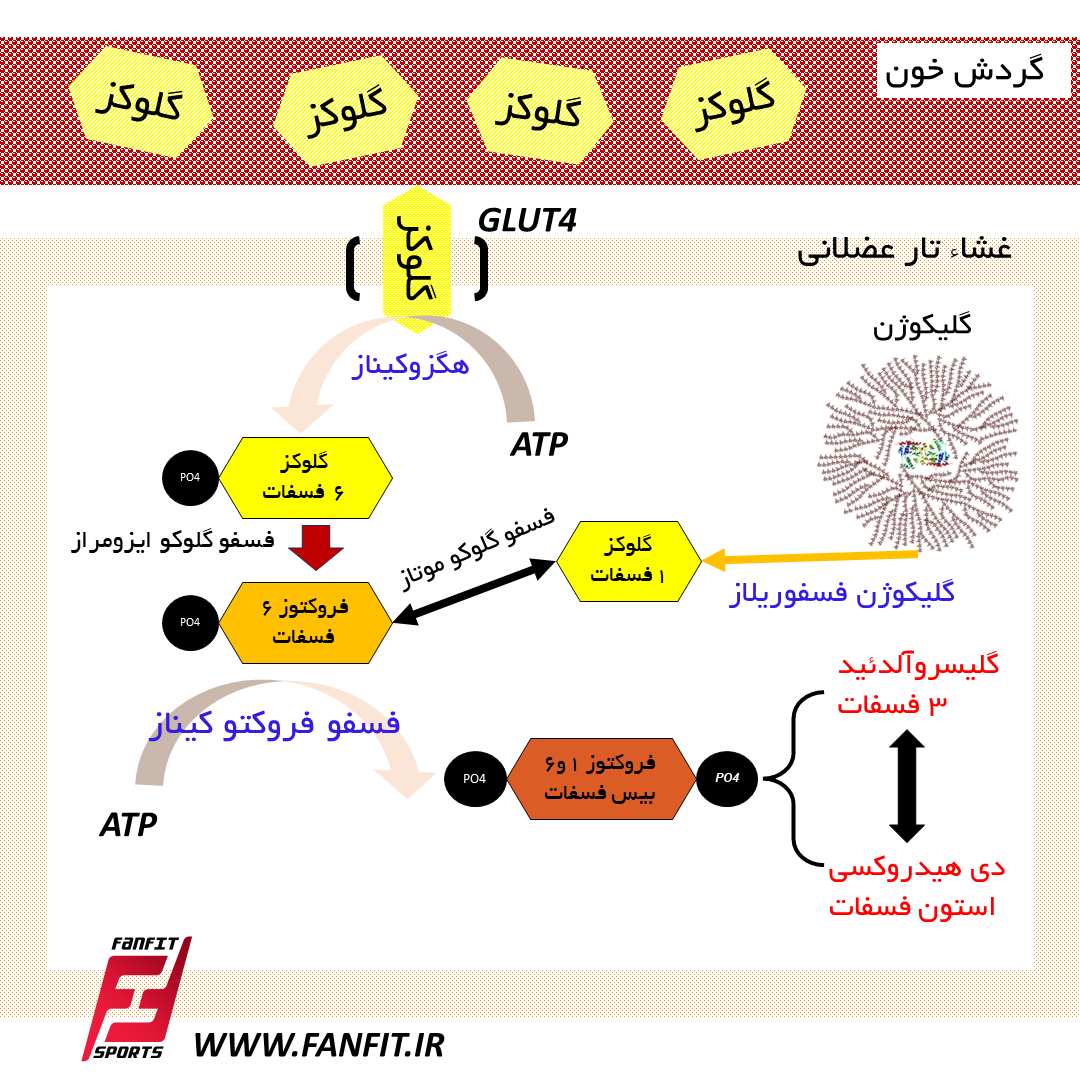
پس یک مولکول گلوکز تا پایان مرحله پنجم، به دو مولکول گلیسرآلدهید ۳-فسفات شکسته میشود. اینجا پایان بخش اول گلیکولیز است (که در آن ATP هزینه شد).
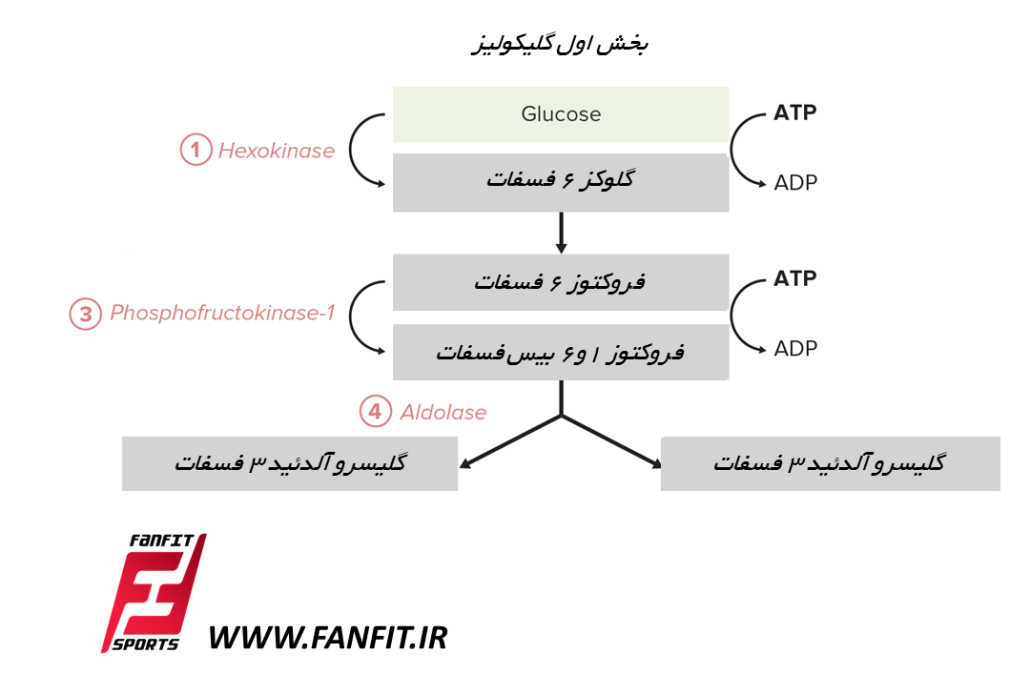
از این جا به بعد بخش دوم گلیکولیز آغاز می شود که در آن انرژی ذخیره شده در پیوندهای پرانرژی گلوکز (که اکنون به دو موکلول گلیسرآلدهید ۳-فسفات تبدیل گردیده) برای تشکیل مولکول های پرانرژی مانند ATP و NADH استفاده میشود. یک گروه فسفاتی آزاد (و نه از ATP) به گلیسرآلدهید ۳-فسفات متصل شده و با انتقال هیدروژن از این ترکیب به NAD+، یک مولکول ۳،۱-بیسفسفوگلیسرات و یک مولکول NADH تشکیل میگردد.
سپس یکی از فسفات های ترکیب ۳،۱-بیسفسفوگلیسرات به ADP منتقل شده و که در نتیجه آن ۳-فسفوگلیسرات و ATP تولید میشود.
با جابهجایی برگشتپذیر گروه فسفاتی بین کربنهای ۲ و ۳ در گلیسرات توسط آنزیم فسفوگلیسرات موتاز، ۳-فسفوگلیسرات به ۲-فسفوگلیسرات تبدیل میشود. آنزیم انولاز با برداشت یک مولکول آب از ۲-فسفوگلیسرات، فسفوانول پیروات را تولید میکند.
فسفوانول پیروات توانایی بالایی در انتقال گروه فسفاتی پرانرژی دارد که در مرحله بعدی از آن استفاده میکند. مرحله پایانی مسیر امبدن – میرهوف، انتقال گروه فسفاتی از فسفوانول پیروات به ADP توسط آنزیم پیروات کیناز و تولید ATP میباشد. پیروات حاصله نیز بسته به شرایط یاخته، وارد مسیرهای دیگری میشود.
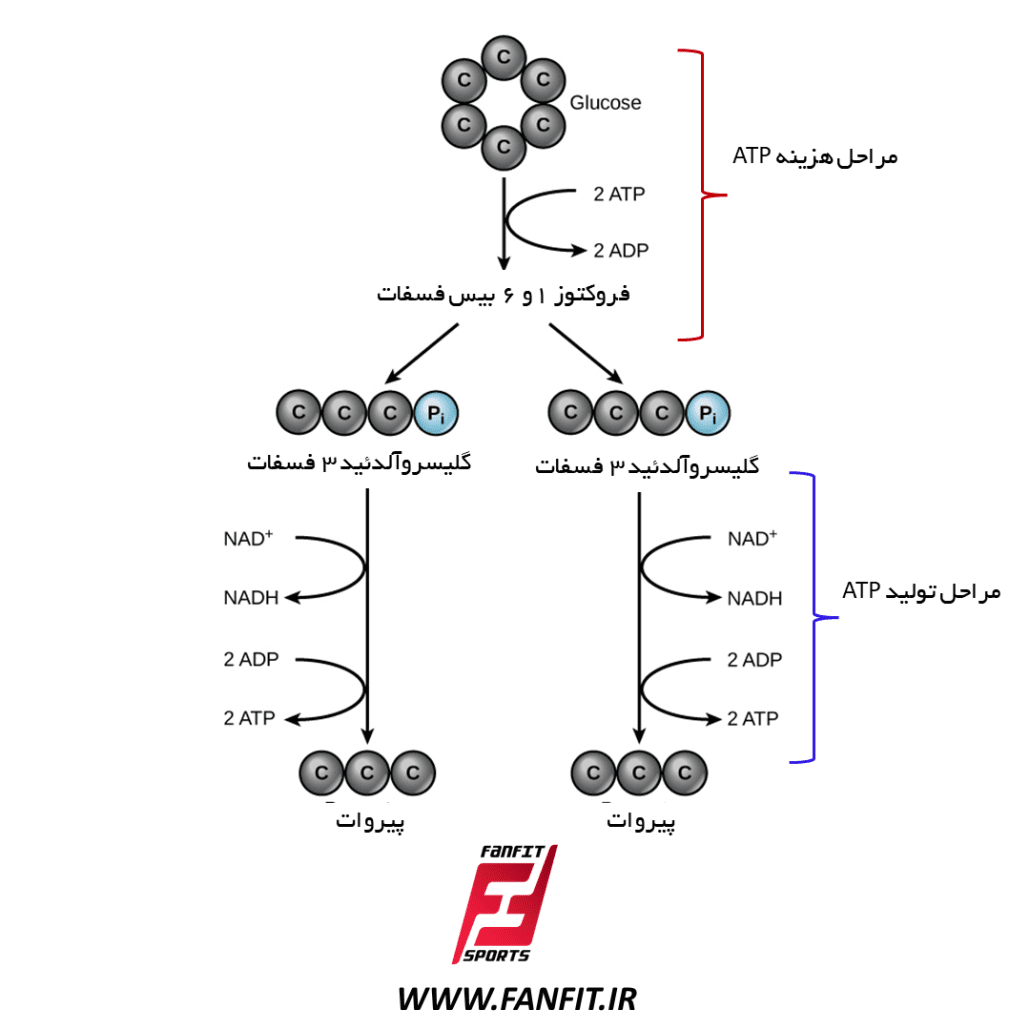
نکته مهم: از واکنش پنجم به بعد هر واکنش دو بار انجام می شود بنابراین در نهایت از هر مولکول گلوکز، ۲ مولکول پیروات و ۲ مولکول NADH و ۴ ملکول ATP تولید می شود. همچنین چون تا قبل از واکنش پنجم، ۲ مول ATP برای پیشرفت گلیکولیز هزینه می شود، این قسمت را مرحله بدهی گلیکولیز می نامند اما چون پس از واکنش پنجم تا واکنش ۱۰، مجموعاً ۴ مولکول ATP بازسازی می شود، به آن مرحله بازپرداخت بدهی می گویند.
بنابراین مجموعاً ATP خالص تولیدی از گلیکولیز به شرطی که گلوکز بیرون سلولی آغازگر گلیکولیز باشد، ۲ مول ATP است. اما اگر گلیکوژن مبدأ گلیکولیز باشد ATP خالص تولیدی برابر با ۳ مول ATP است زیرا تجزیه گلیکوژن شامل واکنش هگزوکیناز نمی شود و در بخش اول گلیکولیز ۱ ATP کمتر هزینه می کند.
واکنش های مهم و محدود کننده سرعت گلیکولیز در سیتوپلاسم
- واکنش ۱، آنزیم هگزوکیناز (ویژه گلوکز خارج سلولی/ خون)
در نخستین مرحله مسیر امبدن – میرهوف، گلوکز با فسفرگیری در کربن شماره شش و تولید گلوکز ۶-فسفات، جهت واکنشهای بعدی فعال میگردد. دهنده این گروه فسفات، ATP است. این واکنش که در شرایط درون سلولی برگشتناپذیر است توسط آنزیم هگزوکیناز کاتالیز میگردد. هگزوکیناز برای فعالیت به یون منیزیم نیازمند است. این آنزیم در تمامی یاختههای موجود در همگی موجودات زنده وجود دارد.
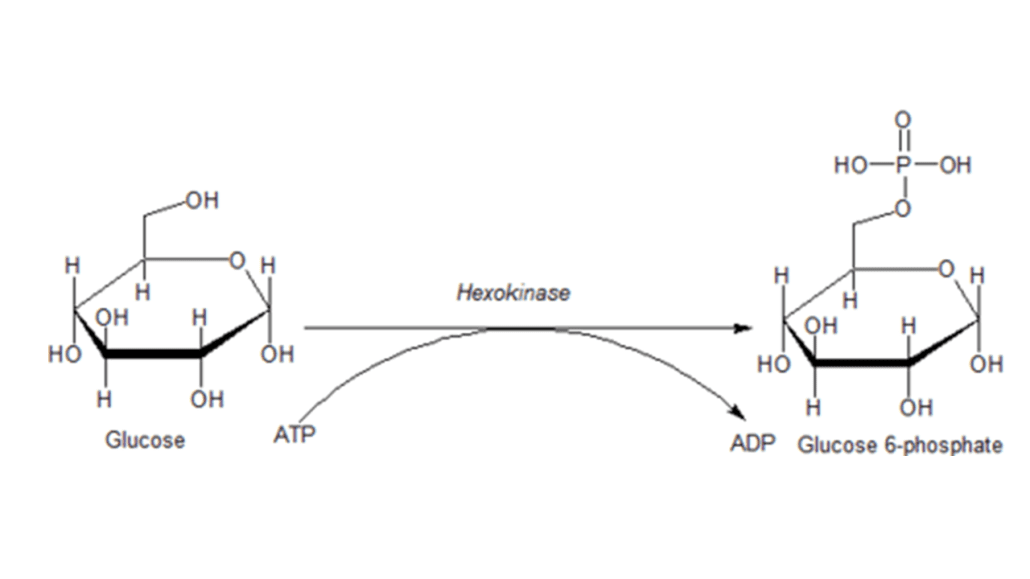
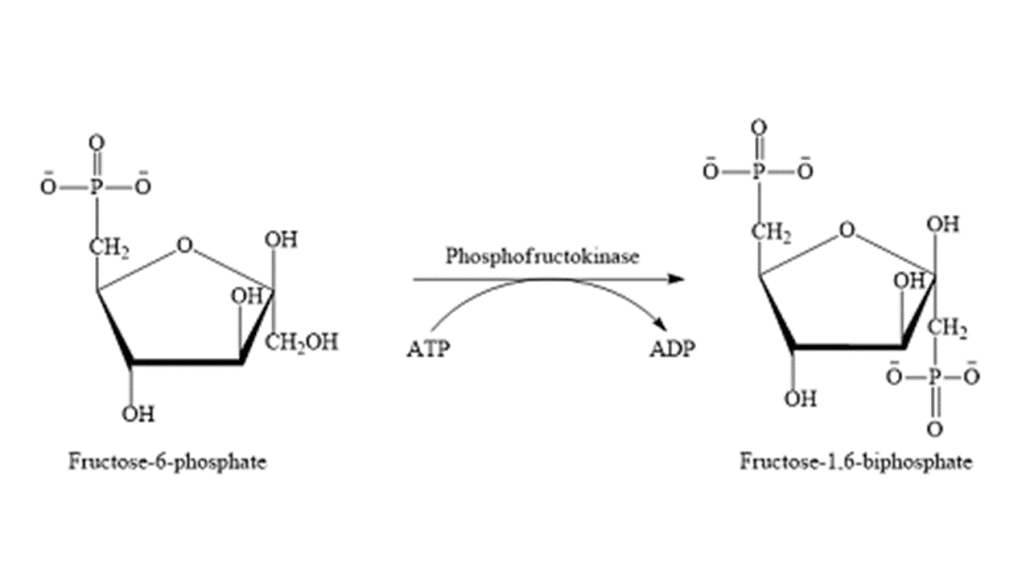
- واکنش ۳، آنزیم فسفوفروکتوکیناز-۱:
با انتقال یک گروه فسفاتی از یک مولکول ATP به فروکتوز ۶-فسفات توسط آنزیم فسفوفروکتوکیناز-۱، فروکتوز ۱و۶ بیسفسفات ایجاد میگردد. این واکنش در شرایط درون سلولی، برگشتناپذیر است. آنزیم فسفوفروکتوکیناز-۱، یکی از آنزیمهای کلیدی مسیر امبدن – میرهوف است.
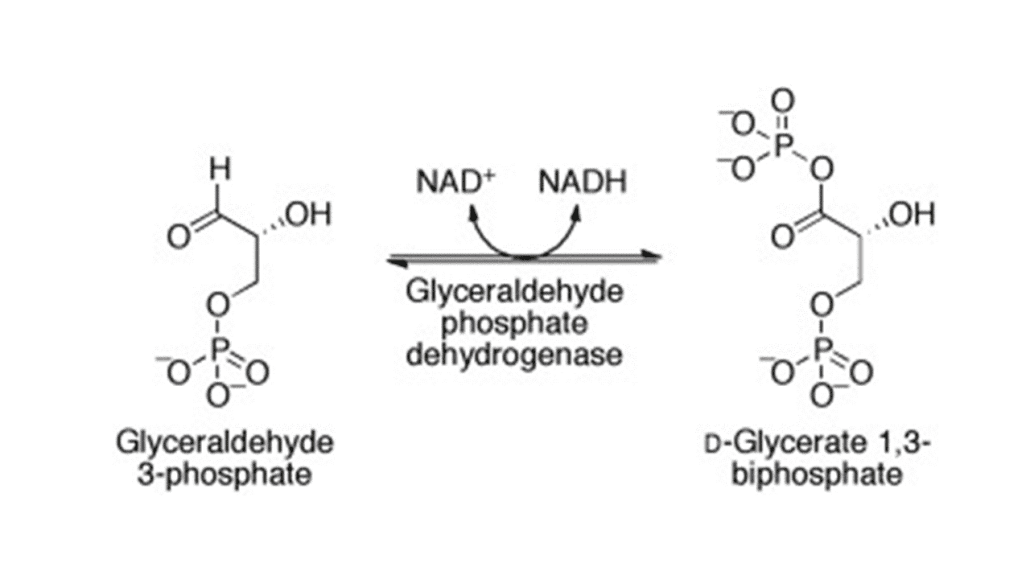
- واکنش ۶، آنزیم گلیسرآلدهید ۳-فسفات دهیدروژناز:
گلیسرآلدهید ۳-فسفات توسط آنزیم گیسرآلدهید ۳-فسفات دهیدروژناز به مولکول ۳،۱-بیسفسفوگلیسرات اکسید میگردد. این واکنش اکسایشی با تولید یک مولکول NADH از NAD+ همراه است. مولکول ۳،۱-بیسفسفوگلیسرات دارای انرژی آزاد هیدرولیز بالایی است به گونهای که در ادامه واکنشها از این ترکیب برای تولید ATP از ADP استفاده میگردد.
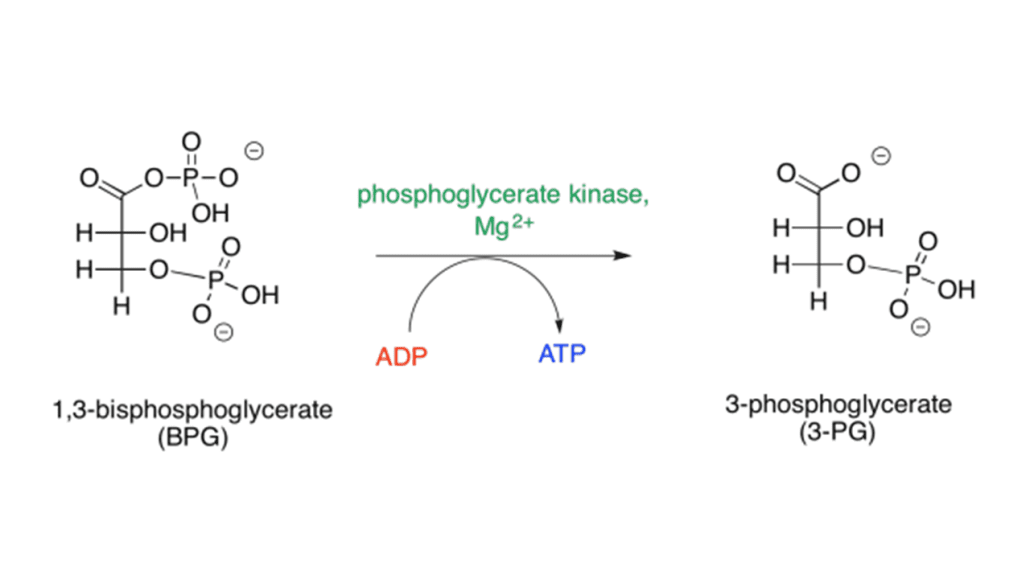
- واکنش ۷، آنزیم فسفوگلیسرات کیناز:
با انتقال گروه فسفاتی از ۳،۱-بیسفسفوگلیسرات به ADP توسط آنزیم فسفوگلیسرات کیناز، یک مولکول ۳-فسفوگلیسرات به همراه ATP تولید میشود. این مرحله، یک واکنش از نوع فسفرگیری در سطح سوبسترا است.این واکنش بر خلاف اکثر واکنشهایی که به وسیله کینازها انجام میگیرد برگشت پذیر است.
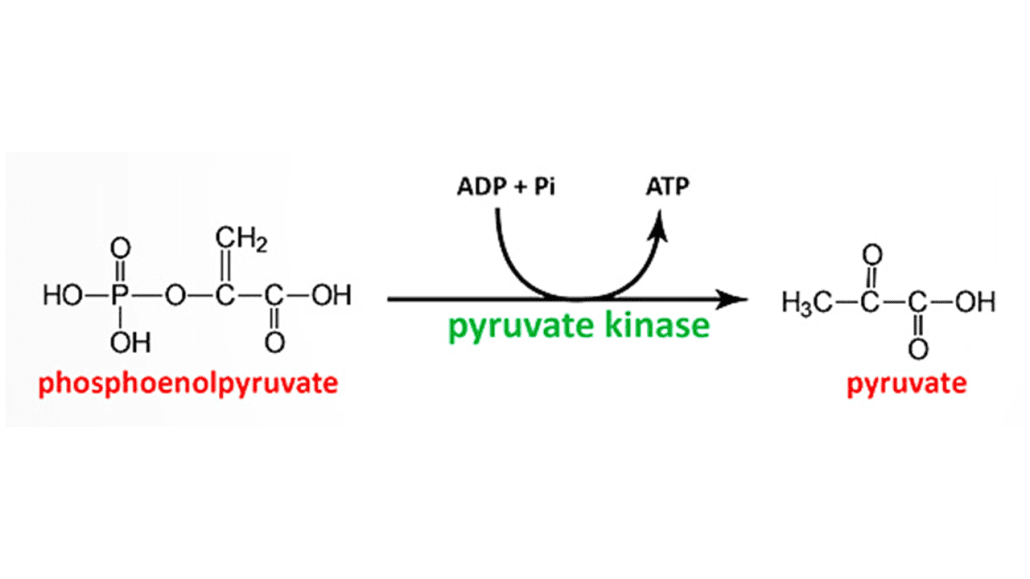
- واکنش ۱۰، آنزیم پیروات کیناز:
مرحله پایانی مسیر امبدن – میرهوف، انتقال گروه فسفاتی از فسفوانول پیروات به ADP توسط آنزیم پیروات کیناز و تولید ATP میباشد. پیروات حاصله نیز بسته به شرایط یاخته، وارد مسیرهای دیگری میشود.
به طور خلاصه:
اگر گلوکز مبداء گلیکولیز باشد = خالص ATP تولیدی ۲ مول می باشد (۴ مول ATP در بخش دوم تولید شد و ۲ مول ATP نیز در بخش اول هزینه شد (در واکنش هگزو کیناز و فسفو فروکتو کیناز) بنابراین ۲=۲-۴)
اگر گلیکوژن مبداء گلیکولیز باشد = خالص ATP تولیدی ۳ مول می باشد (۴ مول ATP در بخش دوم تولید شد و ۱ مول ATP نیز در بخش اول هزینه شد (در واکنش فسفو فروکتو کیناز)، بنابراین ۳=۱-۴
محصولات کلی واکنش آنزیمی گلیکولیز :
- دو یا سه مول ATP
- دو مول NADH
- دو مول پیروات با پیروویک اسید
در تصویر زیر تمامی مراحل آنزیمی گلیکولیز و گلیکوژنولیز ذکر شده است.
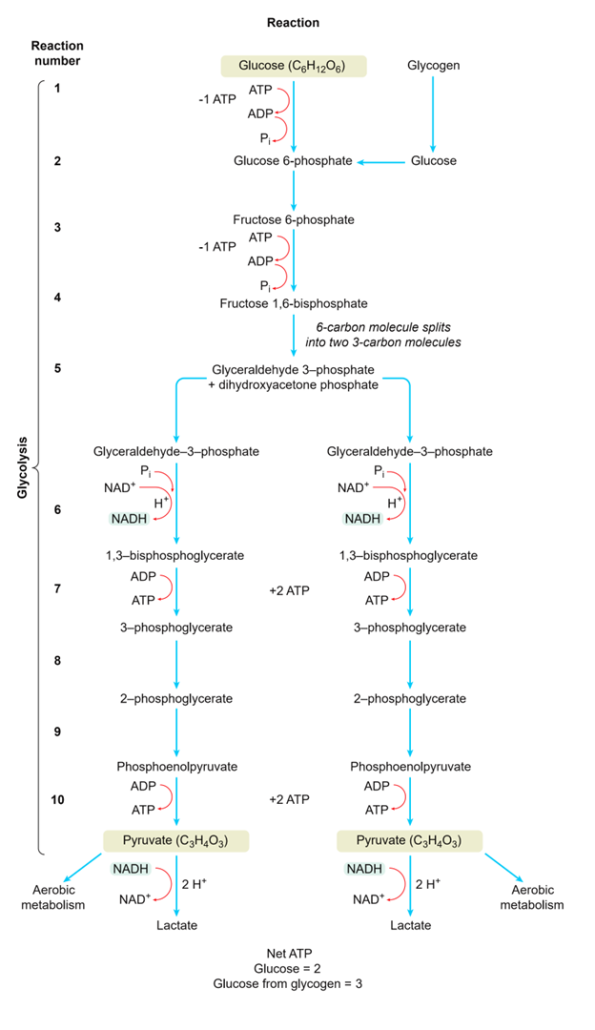
پیروات تولیدی در اثر گلیکولیز وابسته به شرایط سلولی سرنوشت های زیر را می تواند داشته باشد:
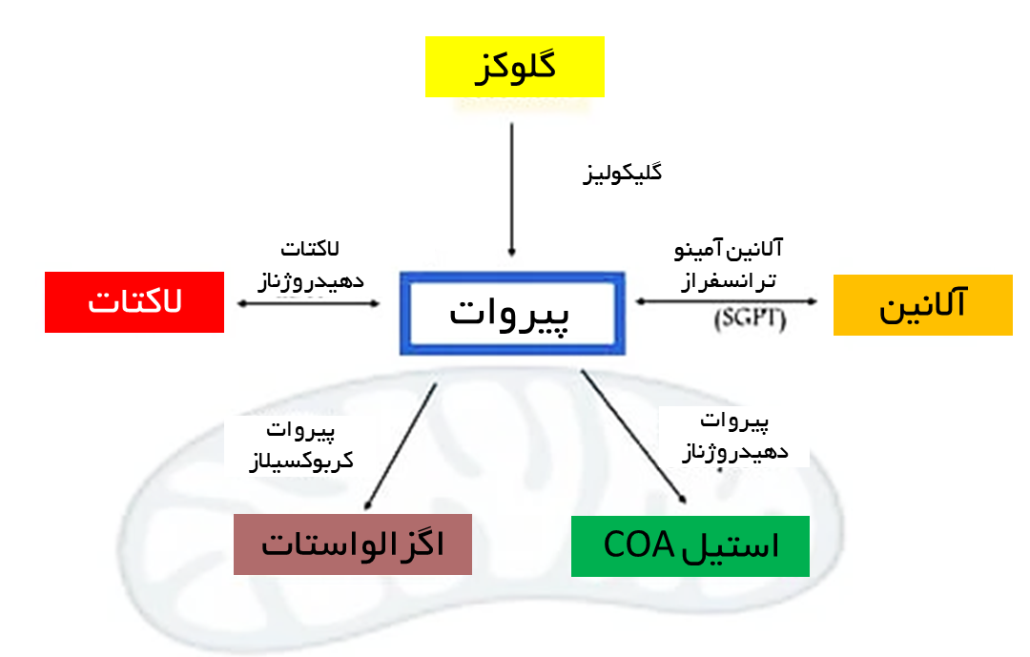
۱- تولید لاکتات از پیروات
تولید لاکتات که ارزش آن نوسازی مجدد NAD است و باعث می شود که روند گلیکولیز حفظ شود. آنزیم کلیدی این واکنش لاکتات دهیدروژناز (LDH) است. این واکنش برگشت پذیر است یعنی می تواند لاکتات را به پیروات نیز تبدیل کند. بنابراین عملکرد آن متاثر از غلظت سوبسترا در هر سمت واکنش است. وقتی که غلظت پیروات زیاد باشد، میل به سمت تولید لاکتات دارد، این موضوع به ویژه در تارهای تند انقباض نوع IIx بارزتر است.
در عوض هنگامی که غلظت لاکتات بیشتر باشند میل به سمت تبدیل آن به پیروات دارد، در تارهای نوع I، لاکتات تولیدی از تارهای نوع II با عملکرد آنزیم لاکتات دهیدروژناز به پیروات تبدیل می شوند و بعد در مسیر هوازی درون میتوکندری ها کاملاً متابولیزه (به استیل کوآ تبدیل می شود) می شود. پس تارهای نوع I قابلیت بافر لاکتات تولیدی در تارهای IIx را دارند.
آنزیم لاکتات دهیدروژناز از پنج ایزوآنزیم تشکیل شدهاست، شامل:
- لاکتات دهیدروژناز ۱ یا LDH-1: که بهطور معمول در قلب،تارهای عضلانی نوع I، سلول های قرمز و مغز موجود است.
- لاکتات دهیدروژناز ۲ یا LDH-2: که بهطور معمول در فاگوسیت های تک هستهای (مونوسیت ها و هم خانواده های آن ها) موجود است.
- لاکتات دهیدروژناز ۳ یا LDH-3: که بهطور معمول در شُشها و سایر بافتها موجود است.
- لاکتات دهیدروژناز ۴ یا LDH-4: که بهطور معمول در کلیهها – جفت (کالبدشناسی) و پانکراس موجود است.
- لاکتات دهیدروژناز ۵ یا LDH-5: که بهطور معمول در کبد و عضلات اسکلتی (تارهای نوع IIx) موجود است.
تولید لاکتات مضر نیست، حتی می تواند هنگام انقباض عضلانی مزایایی نیز داشته باشد.
- سنتز NAD+ سیتوزولی را زیاد می کند ← افزایش تداوم گلیکولیز با سرعت زیاد ← حفظ نوسازی ATP در فعالیت های انقباضی شدید و سریع
- می تواند توسط شاتل های لاکتات، سلول به سلول از تارهای گلیکولیتیک (II) به تارهای اکسیداتیو (I) فعال یا غیر فعال راه یابد و به عنوان یک سوبسترای انرژی مورد استفاده قرار گیرد.
- می تواند از سلول خارج و توسط کبد و قلب مورد استفاده قرار گیرد. در کبد می تواند به عنوان یک پیش ساز گلوکونئوژنیک مورد استفاده قرار گیرد که به آن چرخه کوری می گویند. از این راه لاکتات متابولیزه شده در کبد می توان به حفظ گلوکز پلاسمایی کمک کند.
- می تواند توسط شاتل درون سلولی به درون میتوکندری های همان سلولی که تولید شده راه یابد و اکسید شود.
- لاکتات به عنوان یک مولکول پیام رسان داخل سلولی عمل کرده و می تواند باعث تکثیر و بیوزنز میتوکندریایی شود.
هنگامی که گلیکولیز به سرعت در حال انجام است، مشکل سلول این است که دسترسی به کوآنزیم NAD+ محدود می شود، این کوآنزیم برای واکنش گلیسرآلدئید ۳- فسفات دهیدروژناز (واکنش شماره ۶ گلیکولیز) ضروری است. در واقع هنگامی که گلیکولیز با سرعت زیاد در حال انجام است، مقادیر زیادی از NAD+ به NADH احیا می شوند که نتیجه آن افزایش نسبت NADH/NAD در سیتوپلاسم است.
این تغییر در نسبت NADH/NAD+ باعث مهار ادامه گلیکولیز و تشکیل پیروات می شود. بنابراین اگر NADH تشکیل شده بر اثر گلیکولیز نتواند به میزان متعادلی به NAD+ تبدیل شود؛ امکان ادامه گلیکولیز وجود ندارد. با این حال سلول از دو مسیر برای بازسازی NAD+ استفاده می کند:
- الف: از NADH برای احیای پیروات به لاکتات استفاده می کند و در نتیجه NAD+ را بازسازی می کند.
- ب: با استفاده از دو شاتل مالات آسپارتات، گلیسرول فسفات، الکترون های NADH را به حامل های احیای درون میتوکندریایی (FAD+ و NAD+) منتقل می کند و در نتیجه مقادیر NAD+ سیتوزولی را در سطوح مناسب حفظ می کند.
احیای پیروات به لاکتات توسط لاکتات دهیدروژناز: این واکنش توسط یک آنزیم ویژه به نام لاکتات دهیدروژناز (LDH) انجام می شود. فعالیت این واکنش برگشت پذیر است یعنی می تواند لاکتات را به پیروات نیز تبدیل کند. بنابراین عملکرد آن متاثر از غلظت سوبسترا در هر سمت واکنش است.
وقتی که غلظت پیروات زیاد باشد، میل به سمت تولید لاکتات دارد این موضوع به ویژه در تارهای تند انقباض نوع IIx بارزتر است. در عوض هنگامی که غلظت لاکتات بیشتر باشند میل به سمت تبدیل آن به پیروات دارد، برای مثال در تارهای نوع I، لاکتات تولیدی از تارهای تند با عملکرد همین آنزیم به پیروات تبدیل می شوند و بعد در مسیر هوازی درون میتوکندری ها کاملاً متابولیزه می شود. پس تارهای نوع I قابلیت بافر لاکتات تولیدی در تارهای IIx را دارند.
بازسازی اکسیداتیو NAD+ توسط شاتل های میتوکندریایی: با استفاده از دو شاتل مالات آسپارتات و گلیسرول فسفات، الکترون های NADH به حامل های احیایی درون میتوکندریایی (FAD+ و NAD+) منتقل می شوند و در نتیجه مقادیر NAD+ سیتوزولی را در سطوح مناسب حفظ می شود. با وجود این استفاده از این شاتل های میتوکندریایی برای اکسید کردن NADH فرایندی کند و زمان بر است.
بنابراین نمی تواند هنگامی که NADH در سرعت های زیاد گلیکولیز به مقدار زیاد تولید می شود چندان موثر باشند. اما هنگامی که گلیکولیز به آهستگی به پیش می رود بسیار موثر هستند و می تواند مقادیر بالقوه ای انرژی را از این راه بازسازی کنند. به علاوه فسفوریلاسیون اکسایشی در داخل میتوکندری انجام می شود در حالی که گلیکولیز، NADH را در سیتوپلاسم تولید می کند و غشاء میتوکندری به NADH و NAD+ نفوذ ناپذیر است.
بنابراین مسیر های شاتل میتوکندریایی ویژه زمان هایی است که پیروات برای متابولیسم بیشتر وارد چرخه متابولیسم هوازی در میتوکندری می شود یا به اسید آمینه آلانین تبدیل می شود.
۲- ورود به میتوکندری و تولید استیل کوانزیم A که باعث می شود بین ۳۶ تا ۳۹ مول ATP به واسطه فسفوریلاسیون اکسایشی تولید شود
واکنش اکسایش پیروات در ماتریکس میتوکندری توسط پیروات دهیدروژناز (PDH) کاتالیز می شود. کمپلکس پیرووات دهیدروژناز، یک ترکیب آنزیمی ماتریکس میتوکندری و کدشونده در هسته است که ارتباط اولیه بین گلیکولیز و چرخه اسید سیتریک (چرخه کربس) را از طریق تبدیل برگشتناپذیر پیروویک اسید به استیل-کوآنزیم A یا ACoA فراهم میکند.
واکنش PDH باید با دقت تنظیم شود زیرا تشکیل ACoA از پیروات واکنشی برگشت ناپذیر است. بنابراین تبدیل پیروات به استیل CoA به معنای از دست رفتن پیش ساز بالقوه گلوکز است. در واقع پیروات می تواند در کبد به گلوکز تبدیل شود، اما استیل کوآ نمی تواند. بنابراین برای صرفه جویی در از دست رفتن پیروات لازم است که آنزیم پیروات دهیدروژناز به دقت تنظیم شود.
تنظیم PDH از راه فسفوریلاسیون، دِفسفوریلاسیون و نیز سازوکارهای آلوستریکی انجام می شود. باید یادآور شد، با هر بار طی شدن گلیکولیز، ۲ مولکول پیروات تشکیل می شود، بنابراین به ازای هر ملکول گلوکز ظرفیت تشکیل ۲ مول استیل کوآنزیم A نیز در میتوکندری وجود دارد. هر استیل کوآنزیم A نیز پتانسیل راه اندازی یک چرخه کربس را دارد. بنابراین به ازای هر گلوکز، می توان ۲ چرخه کربس در میتوکندری را فعال کرد.طی تشکیل استیل کوآنزیم A از پیروات توسط PDH نیز ۱ مول NADH نیز تشکیل می شود.
پس از تشکیل استیل کوآنزیم A در اولین مرحله چرخه اسید سیتریک ابتدا استیل کوآنزیم A که مادهای ۲ کربنه است با اگزالو استات که ۴ کربن دارد وارد واکنش شده و کوآنزیم A از آن جدا میشود. محصول نهایی این واکنش Citrate + CoA-SH است. اگزالواستات شروعکننده چرخه کربس، نیز توسط آنزیم پیرووات کربوکسیلاز از پیروات که محصول گلیکولیز است تشکیل میشود.
به طور خلاصه چرخه کربس، مجموعهای از واکنشها است که در آن دو مولکول دی اکسید کربن، یک مولکول GTP/ATP و شکل های احیا شده مولکولهای NADH و FADH تولید میشوند. مانند تبدیل پیروات به استیل کوآنزیم A، چرخه اسید سیتریک نیز در ماتریکس میتوکندری انجام میشود.
تقریبا تمام آنزیمهای چرخه اسید سیتریک محلول در ماتریکس هستند، در این میان فقط آنزیم سوکسینات دهیدروژناز به عنوان یک استثنا است که درون غشای داخلی میتوکندری قرار دارد. برخلاف گلیکولیز، چرخه اسید سیتریک از یک لوپ یا حلقه بسته تشکیل شده است، محصولی که در مرحله انتهایی چرخه تولید میشود، در مرحله اول چرخه مورد استفاده قرار میگیرد.
هشت مرحله از چرخه کربس از مجموعهای از واکنشهای ردوکس، دهیدروژناز، هیدراتاسیون و دکربوکسیلاسیون تشکیل شدهاند که دو مولکول دی اکسید کربن، یک مولکول GTP یا ATP و فرم احیا شده از مولکولهای NADH و FADH2 را تولید میکنند. چرخه کربس، به عنوان یک مسیر هوازی شناخته میشود زیرا دو مولکول تولید شده در این چرخه NADH و FADH2 باید الکترونهای خود را به مسیر بعدی در این سیستم انتقال دهند که همین امر نیازمند استفاده از اکسیژن است.
اگر این انتقال صورت نگیرد، مراحل اکسیداسیون از چرخه اسید سیتریک نیز اتفاق نمیافتد. به این نکته نیز باید توجه کرد که واکنشهای این چرخه تعداد بسیار کمی ATP به صورت مستقیم تولید میکنند و همچنین اکسیژن را به صورت مستقیم مصرف نمیکنند.
محصولات چرخه اسید سیتریک
هر دور از چرخه کربس سه مولکول NADH و یک مولکول FADH2 را تشکیل میدهد. این حاملها با آخرین قسمت تنفس هوازی برای تولید مولکولهای ATP متصل میشوند. یک GTP یا ATP نیز در هر چرخه ساخته میشود. چندین ترکیب از ترکیبات واسطه در چرخه اسید سیتریک میتواند در ترکیب اسیدهای آمینه غیرضروری مورد استفاده قرار گیرند. بنابراین، چرخه دو جهته کار میکند به این معنا که در هر دو مسیر کاتابولیکی و آنابولیکی عمل میکند
از هر بار انجام چرخه کربس محصولات زیر تولید میشوند:
- یک مولکول گوانوزین تری فسفات GTP/ATP
- ۳ مولکول NADH
- ۱ مولکول FADH2
- ۲ مولکول دی اکسید کربن
- بازتولید اگزالواستات
پس از تکمیل چرخه کربس به ازای هر مولکول NADH سه مول ATP (به طور دقیق تر ۲/۵ مول ATP) تشکیل می شود. همچنین به ازای هر مول FADH نیز ۲ مول ATP (به طور دقیق تر ۱/۵ مول ATP) تشکیل می شود. بنابراین بر اساس منابع قدیمی تر هر بار که چرخه کربس طی می شود ۹ مول ATP به واسطه NADH تولیدی و ۲ مول ATP نیز به واسطه FADH تولیدی، در زنجیره انتقال الکترون تشکیل می شود.
۱ مول ATP نیز در خود چرخه کربس تولید شد. بنابراین مجموعاً هر چرخه کربس پتانسیل تشکیل ۱۲ مول ATP را دارد. پس گلیکولیز می تواند با تشکیل ۲ مولکول پیروات و وارد شدن آن ها به مسیر هوازی دو بار چرخه کربس را راه اندازی کند و ۲۴ مول ATP از این طریق تشکیل شود.
۲ مول ATP نیز در بخش سیتوپلاسمی گلیکولیز به طور خالص تشکیل شد که مجموعاً می شود ۲۶ مول ATP. علاوه بر این طی واکنش PDH نیز به هر پیروات، ۱ مول NADH تشکیل می شود. بنابراین از تبدیل ۲ پیروات به استیل کوآ نیز ۲ NADH تشکیل می شود که می تواند ۶ مول ATP دیگر نیز با ورود به زنجیره انتقال الکترون تولید کند.
بنابراین ۲۶ + ۶ برابر است با ۳۲ مول ATP. سرانجام اگر خاطرتان باشد ۲ مول NADH نیز در بخش سیتوپلاسمی گلیکولیز تشکیل می شد که بستگی دارد به چه طریقی الکترون های خود را به زنجیره انتقال الکترون برساند: اگر با شاتل مالات آسپاراتات این کار را انجام بدهد به ازای هر NADH سه مول ATP و اگر با شاتل گلیسرول فسفات این کار را انجام بدهد به ازای هر NADH دو مول ATP تولید می کند.
بنابراین اگر حامل الکترون های NADH سیتوپلاسمی به زنجیره انتقال الکترون مالات آسپارتات باشد مجموعاً گلیکولیز هوازی (با مبداء گلوکز) می تواند ۳۸ مول ATP و با مبداء گلیکوژن ۳۹ مول ATP تولید کند. اما اگر حامل الکترون های NADH سیتوپلاسمی به زنجیره انتقال الکترون گلیسرول فسفات باشد، مجموعاً گلیکولیز هوازی با مبداء گلوکز می تواند ۳۶ مول ATP و با مبداء گلیکوژن می تواند ۳۷ مول ATP تولید کند.
۳- تولید آلانین
۴- تولید اگزالواستات
۵- خروج از سلول: پیروات فسفوریله نمی باشد، بنابراین می تواند از سلول خارج شود اما بیشتر آن متابولیزه می شود
آشنایی بیشتر با پیروویک اسید:
یک آلفا کتواسید سه کربنه با فرمول شیمیایی «C3H4O3» است که یکی از فراوردههای گلیکولیز و پیشساز اسید آمینهی آلانین میباشد. پیروویک اسید از گلیکولیز گلوکز یا گیلکوژن تولید میشود. پیروویک اسید (و تقریباً همه ترکیبات اسیدی دیگر) در داخل سلول های موجودات زنده به شکل یونی خود، یعنی پیروات (C3H3O3–)، وجود دارد. پیروات تولیدی از گلیکولیز می تواند به درون میتوکندری وارد شده و در اثر آنزیم پیروات دهیدروژناز فعال (PDH دِفسفوریله)، کربن دی اکسید و استیل کوآنزیم A (ترکیب ۲ کربنی) را تولید کند.
تبدیل پیروات به استیل کوآنزیم A باعث می شود که مسیر گلیکولیز بتواند با فسفوریلاسیون اکسایشی در میتوکندری جفت شود و درنتیجه مقادیر زیادی ATP را تولید کند. با این حال، این مسیر معمولاً به کندی پیش می رود و از این رو در فعالیت های ورزشی خیلی شدید، میل پیروات به سمت تشکیل لاکتات است، اما در فعالیت های طولانی مدت و با شدت متوسط می تواند به عنوان یک مسیر بازسازی انرژی مهم مورد توجه قرار گیرد.
آشنایی بیشتر با NAD
NAD یا نیکوتین آمید آدنین دی نوکلئوتید: حامل الکترون به زنجیره انتقال الکترون است و بنابراین، شکل بالقوه ای از انرژی تلقی می شود. هر NAD+ (الکترون از دست داده = اکسید) وقتی به NADH احیا (الکترون به دست آورده = احیا) می شود معادل ۳ (یا ۲.۵) مول ATP تلقی می شود. انرژی ذخیره در این NADH فقط در زنجیره انتقال الکترون آزاد می شود و بنابراین هر جایی که NAD+ به NADH احیا شد باید انرژی آن به روش هوازی (میتوکندری) آزاد گردد.








دیدگاه خود را ثبت کنید
تمایل دارید در گفتگو شرکت کنید؟نظری بدهید!